Konfigurasi Elektron
Konfigurasi elektron adalah susunan elektron berdasarkan kulit atau orbital dari suatu atom. Jadi ada dua cara menyatakan konfigurasi elektron.
Gambar tersebut adalah urutan tingkat energi kulit dan subkulit suatu atom. Ada 4 subkulit yaitu s, p, d, dan f dan angka sebelum subkulit menunjukkan kulit. Subkulit 1s punya tingkat energi paling rendah, lalu naik ke subkulit 2s, 2p, 3s, 3p, sampai terakhir yang paling tinggi 8s. Pastinya elektron yang bisa mengisi subkulit tertentu juga terbatas. Elektron yang mengisi subkulit ini dituliskan dalam bentuk pangkat. Subkulit s maksimal terisi 2 elektron 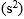 , p terisi 6 elektron (p6), d terisi 10 elektron
, p terisi 6 elektron (p6), d terisi 10 elektron 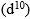 , dan f terisi 14 elektron
, dan f terisi 14 elektron 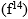 .
.
Saat menuliskan konfigurasi elektron, kita harus menuliskannya secara urut berdasarkan tingkat energi subkulit dari yang terendah ke tertinggi.
Contoh konfigurasi elektron atom karbon.
Karbon punya 6 elektron. Cara menuliskan konfigurasi untuk 6 elektron yang menempati suatu subkulit bisa dilihat dari pangkat subkulitnya. Kalau kita jumlahkan pangkatnya dari 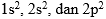 maka pas 6 kan?
maka pas 6 kan?
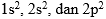 maka pas 6 kan?
maka pas 6 kan?Jadi, dalam menuliskan konfigurasi elektron, ikuti saja urutan tingkat energi kulit dan subkulitnya sampai pangkatnya sama seperti banyaknya elektron yang dipunyai atom itu.





Tidak ada komentar:
Posting Komentar